政策法规||公开征求《申办者临床试验期间安全性评价和安全性报告技术指导原则(附本周法规概览07.11-07.15)
发布时间:2022-07-15
01
关于公开征求《申办者临床试验期间安全性评价和安全性报告技术指导原则(征求意见稿)》意见的通知
随着《药物警戒质量管理规范》的发布和实施,申办者应建立完善的药物警戒体系,对临床试验期间的安全风险管理承担主体责任,以充分保护受试者安全。为更好地推动和指导申办者对临床试验期间的安全性信息及时评价和报告,明确技术标准和向监管机构报告的要求,药审中心遵照国内法律法规要求,同时借鉴国际相关技术指南制定本指导原则。临床试验期间的安全性评价主要是通过个例安全性报告的评价和安全性数据的汇总分析评价来进行汇总分析。
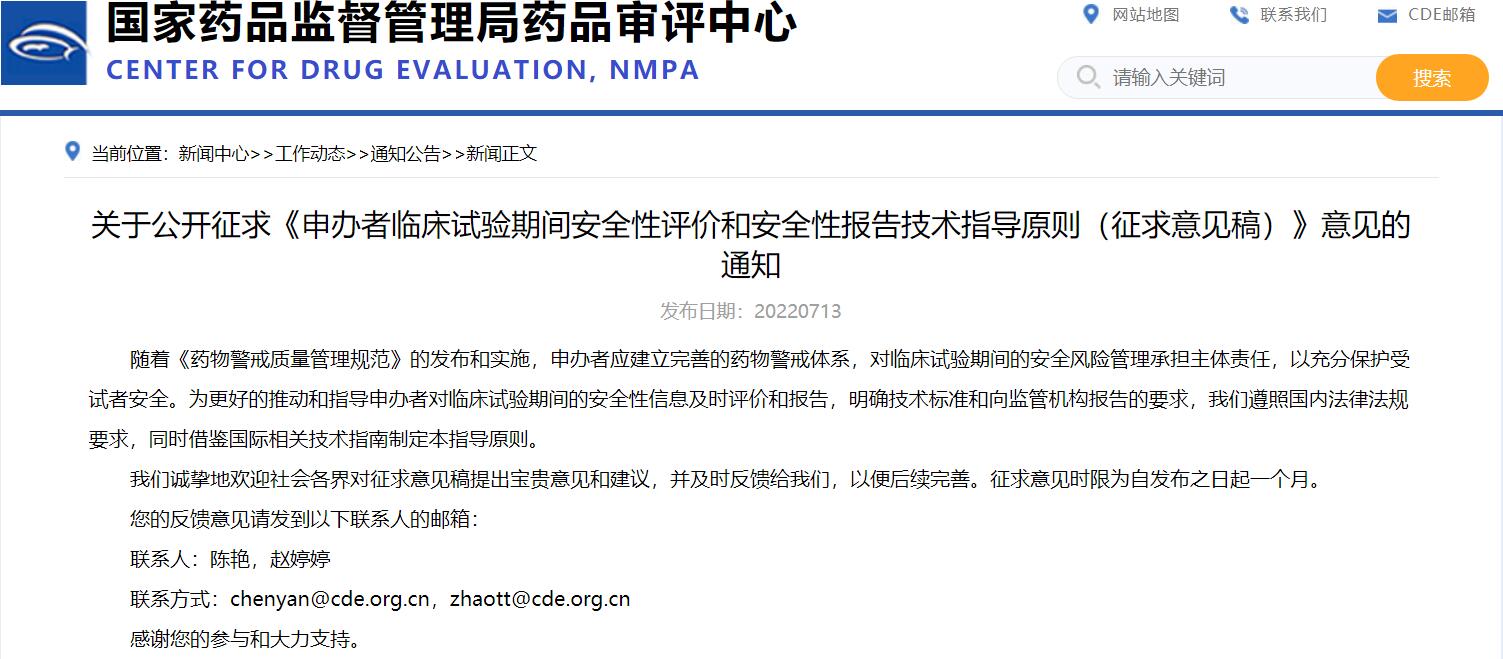
长按识别图中二维码
查看详细信息

NMPA
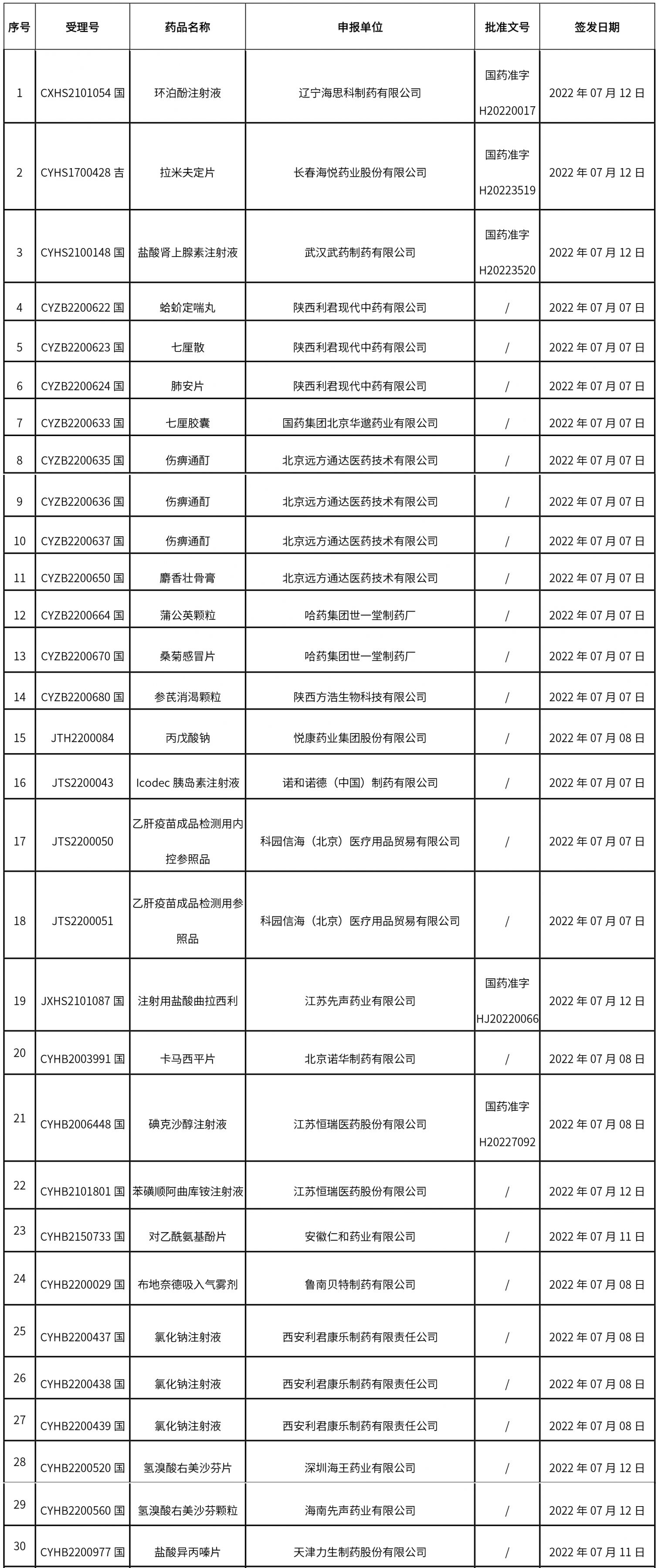
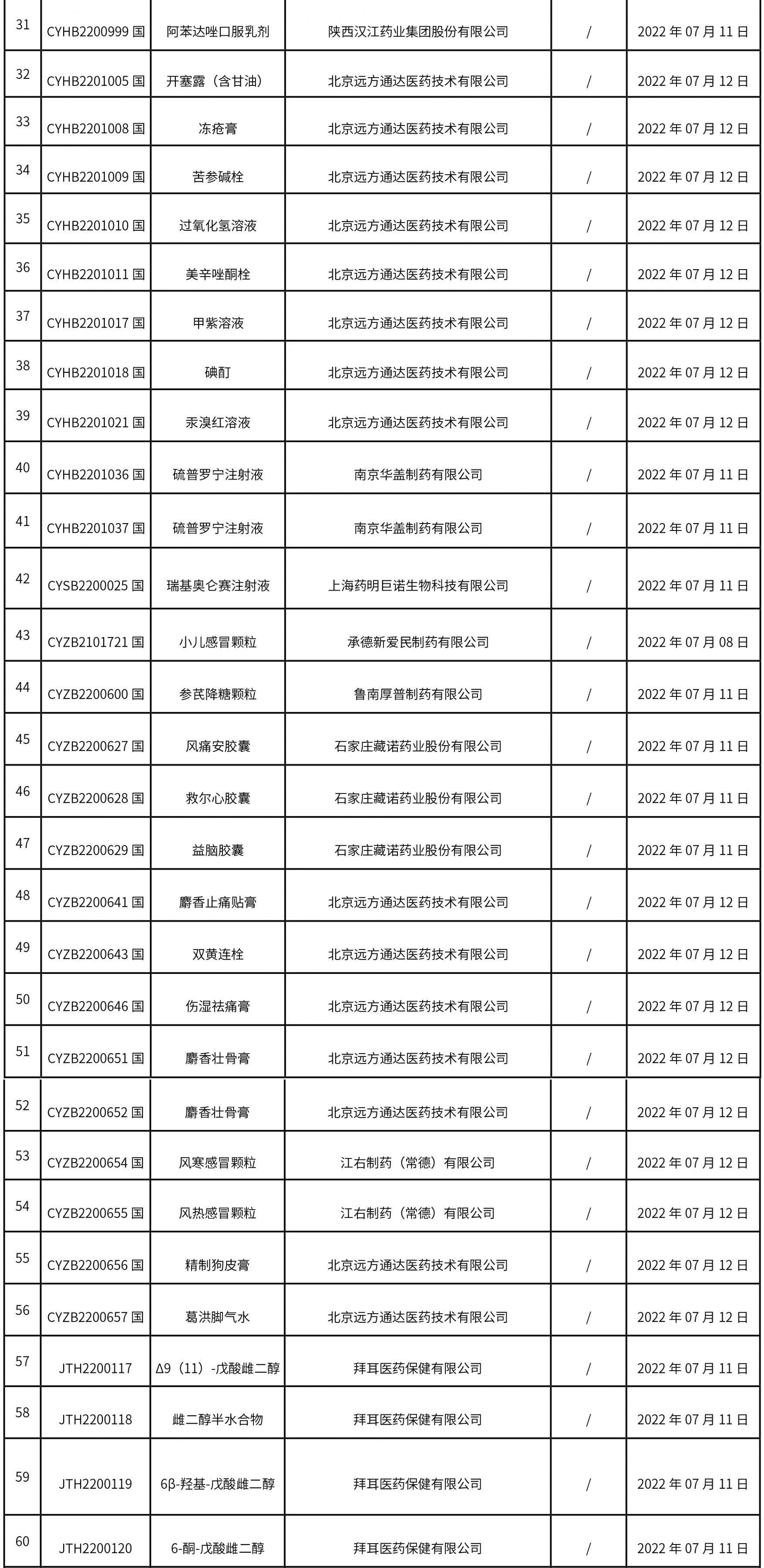
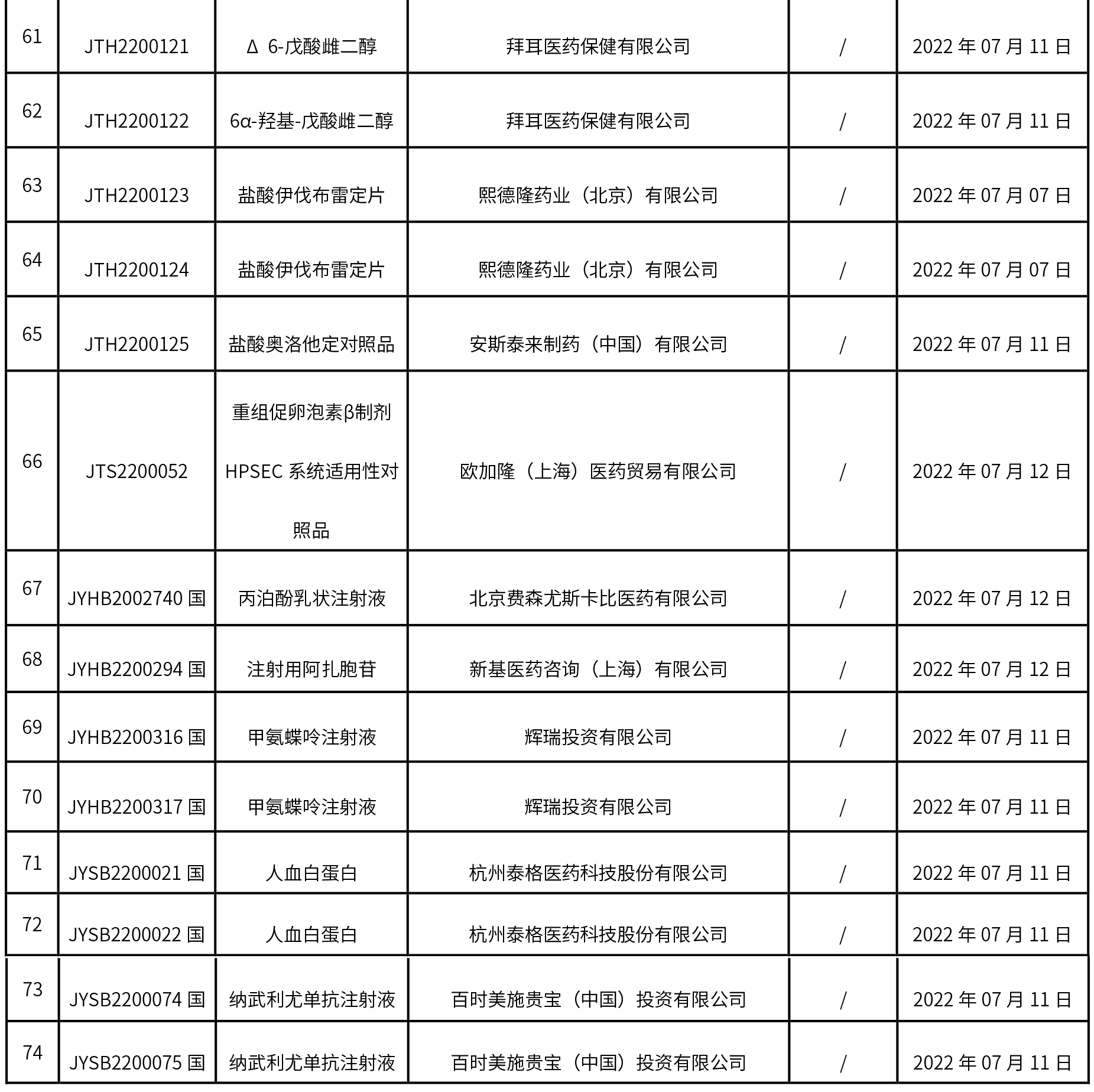
1. 本周共发布了74个品规的药品批准证明文件待领取信息,其中一致性评价1个,注射剂17个。
药典委
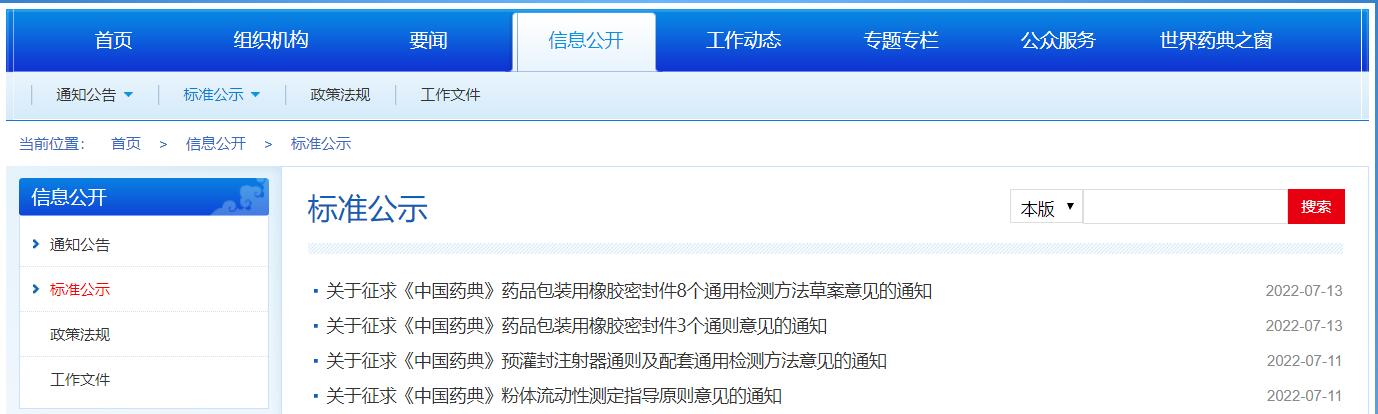
1. 发布1个药用辅料粉体流动性测定指导原则、1个预灌封注射器通则及配套通用检测方法、药品包装用橡胶密封件3个通则和8个通用检测方法草案。
长按识别图中二维码
查看详细信息

-END-



转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文

 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450
