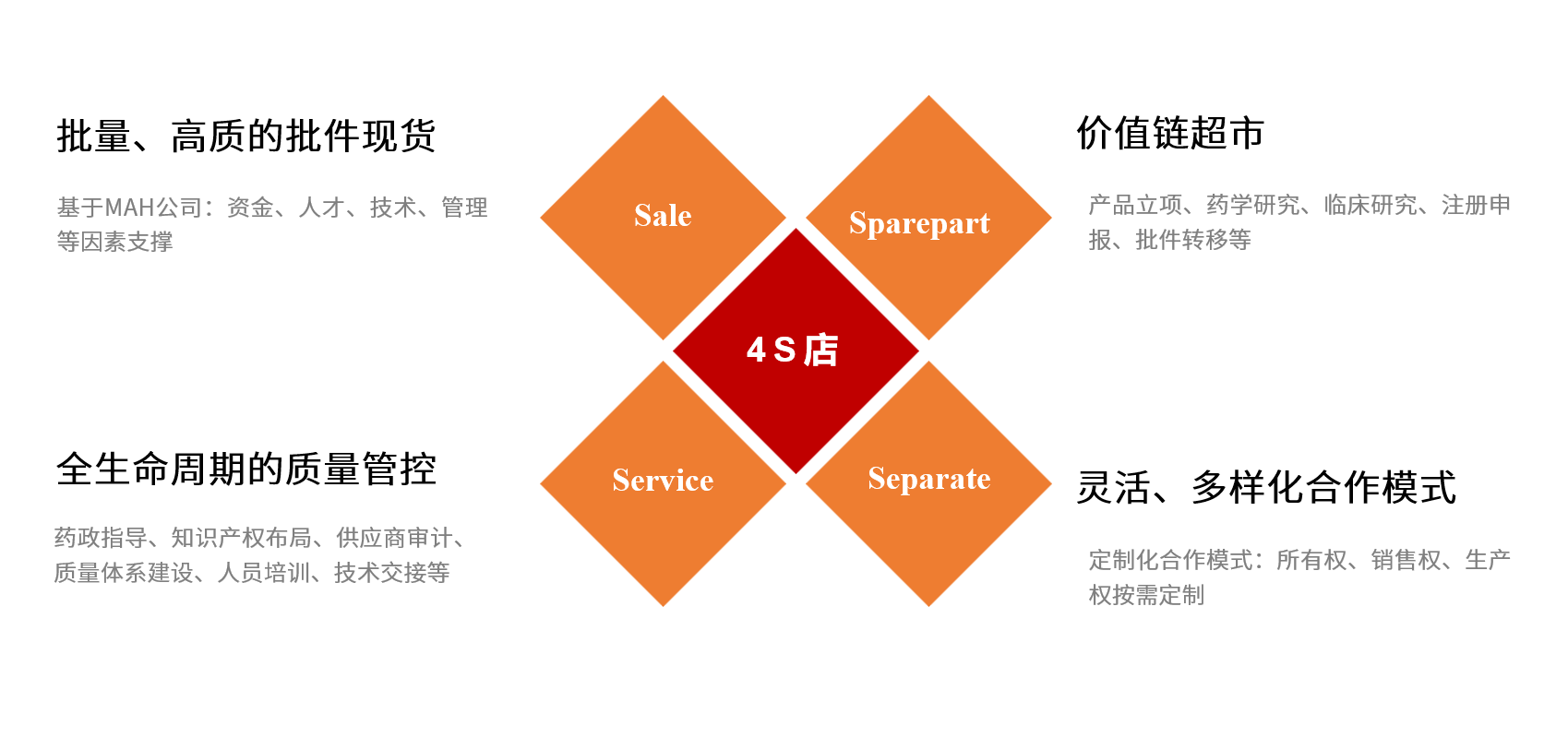
新领先“MAH超市”——产品推介02期
相关链接:
品种介绍

规格:1mg
注册分类:2.2类
参比制剂:改剂型品种,选择规格1mg片剂作为参比制剂,片剂参比已公布(第24批原研进口)。
适应症:适用于原发性帕金森病患者的单药治疗,以及伴有剂末波动患者的联合治疗(与左旋多巴合用)。
临床优势:雷沙吉兰对MAO-B的抑制作用具有强效、高选择性、不可逆性,对帕金森患者疗效显著,优于同类品种司来吉兰,口崩片无需用水送服,在口腔中迅速溶解,解决了片剂需要以水送服,吞咽困难患者和精神疾病患者的顺应性差等问题。
市场销量:口崩片暂未上市,无销量。2022年国内雷沙吉兰制剂销量(公立医疗系统+实体药店)达到1.76亿元,整体需求量较大。
中标价格:国内暂未上市,无中标价
集采价格:未进集采
市场优势:雷沙吉兰是第二代单胺氧化酶抑制剂,与第一代药物相比抑制作用强5-10倍。长效药物,服药便捷,每日1片;国内2022年雷沙吉兰制剂总销量达到1.76亿元,需求量较大,口崩片与片剂相比,对于吞咽困难患者和精神疾病患者依从性更好;目前暂无申报动态,竞争压力小;新领先本项目已获临床默示许可,进度领先,可快速实现技术成果转化。
新领先进度:获得临床默许
规格:240mg
注册分类:4类
参比制剂:参比已公布(第66批原研进口)
适应症:用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒(CMV)血清学阳性的成人受者[R+]预防巨细胞病毒感染和巨细胞病毒病。
临床优势:新型非核苷巨细胞病毒(CMV)抑制剂,FDA的孤儿药资格和优先快速通道,填补了移植后预防领域的空白;与DNA 聚合酶抑制剂相比,来特莫韦对CMV选择性更高,作用强度也有明显提高,抗病毒活性相比更昔洛韦约高1000倍;与安慰剂相比,来特莫韦无髓抑制、肾毒性事件增加,且与更昔洛市等传统抗CMV药物无交叉耐药,无需对轻中重度肾功能损害要者和轻中度肝功能损害患者调整给药剂量;口服给药方便,不直接损伤皮肤或黏膜,具有经济且安全的优点。
市场销量:2023年来特莫韦片国际销量6.54亿美元,同比+36.73%;来特莫韦片国内公立医疗系统2022Q3开始销售,Q3销量71万元,Q4销量430万元;2022年零售药店销量2616万元。随着市场准入地位的提升,有望实现快速放量。
中标价:420-1280元/片
集采价格:暂未进入集采
市场优势:机制创新,具有高度特异性,抗病毒活性高;不良反应少,安全耐受、无交叉耐药性;潜在竞争家数5家,竞争压力较小;国际市场容量较大,增速快,国内目前处于市场初期,已纳入乙类医保,市场前景较好。
新领先进度:预BE
03
规格:240mg/12mL
注册分类:4类
参比制剂:参比已公布(第68批原研进口)
适应症:用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒(CMV)血清学阳性的成人受者[R+]预防巨细胞病毒感染和巨细胞病毒病。
临床优势:新型非核苷巨细胞病毒(CMV)抑制剂,FDA的孤儿药资格和优先快速通道,填补了移植后预防领域的空白;与DNA 聚合酶抑制剂相比,来特莫韦对CMV选择性更高,作用强度也有明显提高,抗病毒活性相比更昔洛韦约高1000倍;与安慰剂相比,来特莫韦无髓抑制、肾毒性事件增加,且与更昔洛市等传统抗CMV药物无交叉耐药,无需对轻中重度肾功能损害要者和轻中度肝功能损害患者调整给药剂量。《2021年NCCN 指南)推荐用作AI-HSCT后CMV感染高风险受者监测期间的一级预防方案。与来特莫韦片剂互补,帮助在治疗过程中存在口服药不耐受现象的部分患者提高药物吸收效率,减少口服吸收较差的患者发生突破性感染的可能。
市场销量:2023年国际销量2696.58万美元,同比+24.25%;国内目前仅零售药店销售,2022年销量10万元。
中标价:430元/瓶-1600元/瓶(12ml:240mg规格)
集采价格:暂未进入集采
市场优势:机制创新,具有高度特异性,抗病毒活性高;不良反应少,安全耐受、无交叉耐药性,与片剂互补,覆盖口服不耐受人群,扩展造血干细胞移植后预防用药范围,临床推荐一线预防方案;竞争压力较小,有望前5家获批;近五年国际销量持续增长,国内目前处于市场初期,已纳入乙类医保,市场前景较好;无需开展验证性临床和BE试验,回报周期短。
新领先进度:中试
规格:175μg/3ml
注册分类:3类
参比制剂:参比已公布(第33批美国橙皮书)
适应症:慢性阻塞性肺疾病(COPD)患者的维持治疗
临床优势:雷芬那辛是首个也是唯一一个被FDA批准用于治疗COPD的每日一次雾化支气管扩张剂;比噻托溴铵或格隆溴铵更高的肺选择性;不会产生全身性抗胆碱能副作用;与噻托溴铵相比,雷芬那辛具有作用持续时间长,副作用小等优势。
市场销量:本品暂无国内销量,国际销量自上市以来持续增长,2023年的全球销售额为2.98亿美元,同比增长+13.9%。
中标价格:国内未上市,无中标价
集采价格:未进集采
市场优势:市场前景好,竞争压力小;临床疗效好,副作用小,每天一次使用方便;原研已完成三期临床即将上市,可待原研进口后按照4类申请上市,无需开展临床试验。
新领先进度:工艺验证
规格:50mg
注册分类:3类
参比制剂:参比已公布(第73批美国橙皮书)
适应症:适用于治疗肌萎缩侧索硬化症 (ALS)
临床优势:可以有效延长患者中位生存期3个月;口溶膜剂型较片剂起效更快,更适用于吞咽困难的患者,可有效替代片剂。
市场销量:口溶膜2023年国际销量104.6万美元,尚处于起步阶段;国内暂无口溶膜上市,片剂2022年销量为1.33亿元(医院+药店),国内近几年销量较稳定。
中标价格:国内未上市,无中标价
集采价格:未进集采
市场优势:片剂在国内近几年销量稳定超亿元,竞争压力小,有望首仿,口溶膜起效更快,更适合吞咽困难患者,可替代片剂;无需开展验证性临床。
新领先进度:预BE
诚邀合作,联系我们 !
张先生 18600750399
张女士 18612403006
张先生 16600205614
-END-


转载声明:未经本网或本网权利人授权,不得转载、摘编或利用其他方式使用上述作品。已经本网或本网权利人授权使用作品的,应在授权范围内使用,并注明“来源:新领先医药科技”。

 Hotline服务热线:010-61006450
Hotline服务热线:010-61006450
 简体中文
简体中文

 010-61006450
010-61006450 联系地址:
联系地址: 技术市场部:
技术市场部: 北京新领先
北京新领先 新领先药讯
新领先药讯 010-61006450
010-61006450
